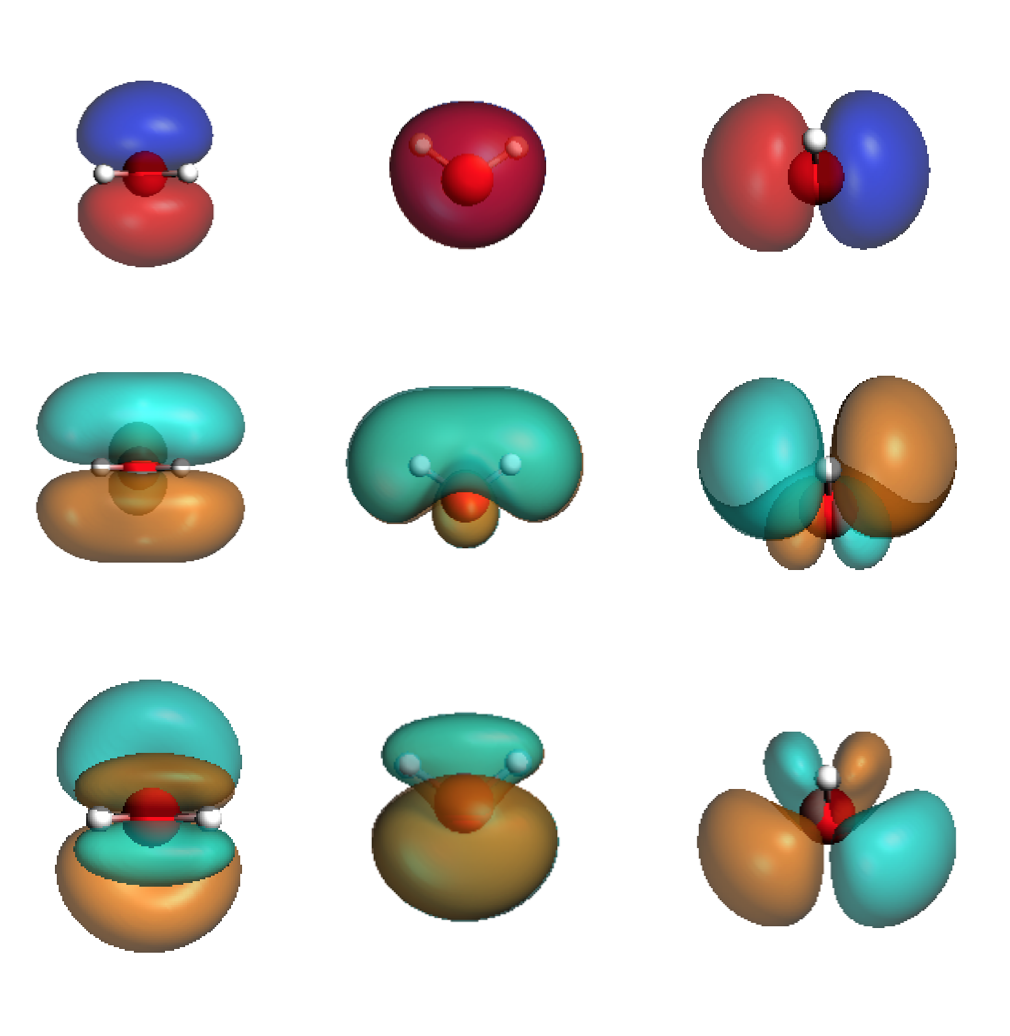这是本文档旧的修订版!
分子对称性、点群与不可约表示、轨道对称性的通俗化理解
点群
当整个分子具有对称性的时候,比如水分子,具有镜面对称、二重转动轴对称,这种对称用一个符号来代表叫做C2v。分子的不同的对称性,用不同的点群名称来代表。对称、点群,有专门的书籍介绍,这里不讲,并且不记得也并不十分妨碍下面的内容。
没有对称性,点群名字为C1,这个需要记住。
ADF的Input窗口底部★按钮可以检测分子的最高点群,(此时坐标会有所调整,轻微的偏差也会被纠正到完全对称),Details → Symmetry中点群设置为Auto即可,ADF计算过程中将采用检测到的点群,结构优化过程也会保持点群不变。
不可约表示
具有对称性的分子,它的分子轨道(MO)也具有对称性,根据分子所属的点群不同,MO的对称性也有不同的类别。但只要分子的点群(也就是对称性)确定之后,MO的对称性也就预先就能知道。知道分子的点群后,MO按对称性可以分为几类也就知道了。而这里所说的MO对称性的归类,就是所谓的不可约表示。
我们以水分子为例来说明:
水分子的对称性是C2v点群。通过查表,可以查到C2v群有4个不可约表示,分别命名为A1、B1、B2、A2(其他点群的不可约表示的名字也基本都是类似的符号,常见的字母有A、B、E、T、Delta、Pai、SIGMA)。其中A、B是不简并的,也就是说归属于A1不可约表示类轨道,每个能级,都只有一个MO,一个MO最多占据2个电子(Spin α、β各1个);E是二重简并的,也就是说,每个能级,都有2个能量完全一致的MO,这样,每个E不可约表示里面的能级,其实对应着2个MO,也就是最多能占据4个电子(Spin α、β各2个);类似的,T是三重兼并的。另外,对于球对称的情况(单个原子),不可约表示的名字,大家可能就熟悉了,叫做S、P、D、F等等。如果分子没有任何对称性,点群为C1,那么不可约表示就只有一个,叫做A,MO也没有任何对称性。
ADF计算过程中,logfile里面会提醒本计算使用的是什么点群:
在out文件中也有相关内容。
分子轨道的对称性
不可约表示,代表的是MO的对称特征
我们形象的来看看H2O:
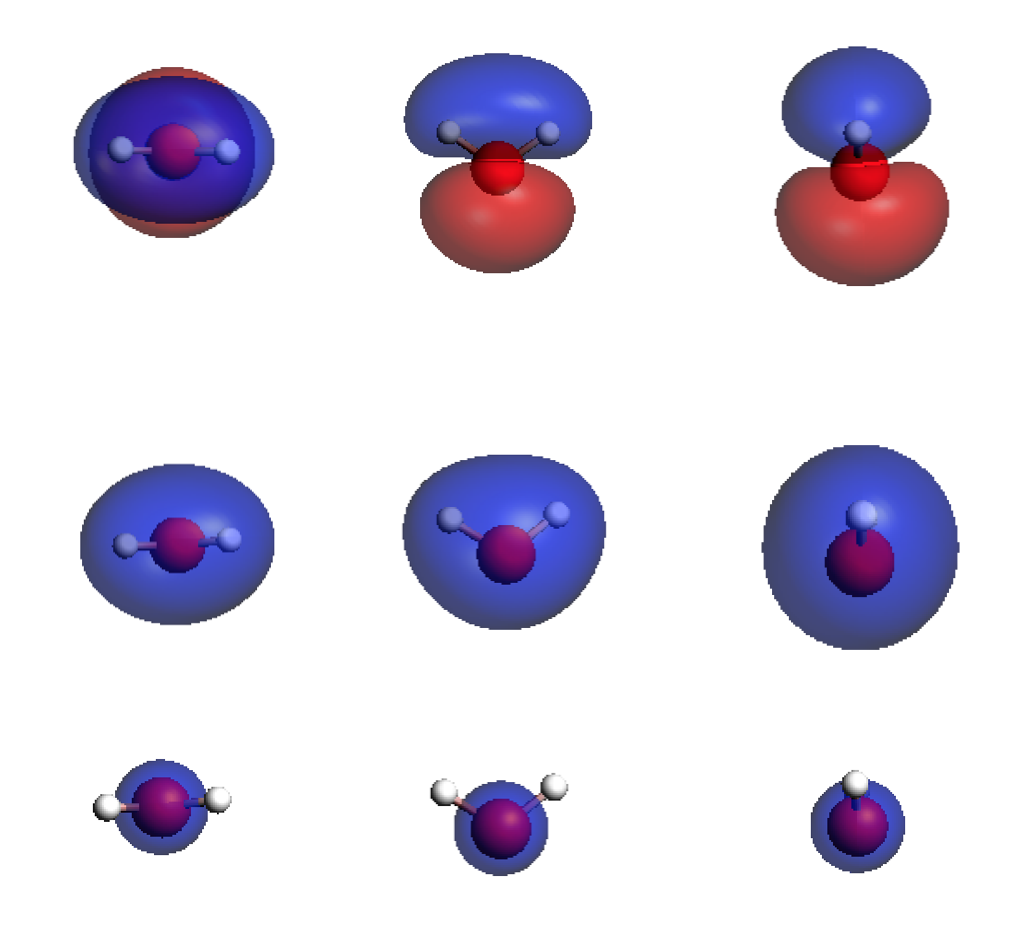
1)A1不可约表示的三个占据轨道(每行为一个轨道,左、中、右是不同的视角。最下面的能量最低)的对称特征——有两个镜面:
空轨道
2)B1不可约表示的1个占据轨道和2个空轨道(能量从上到下升高),特征——一个镜面对称,一个镜面相位相反:
类似地,所有的不可约表示,都类似地具有同种对称特征。
类似地,镜面对称的分子,点群为Cs,轨道按对称性分类,可以分为两类,在ADF中,分别命名为AA(标准名称为A')和AAA(标准名称为A'')。
点群与对应的不可约表示查询
用户可以登陆:
http://www.webqc.org/symmetrypointgroup-cs.html
查询每个点群所对应的不可约表示,例如C2v群的不可约表示,包含A1、B1、B2、A2:
在ADF软件中,命名与此类似,可以查阅此表与ADF的结果对应。
每个不可约表示的电子占据情况
哪些不可约表示需要注意?P、D、F、E、T、Pi、Delta的简并度分别为:3、5、7、2、3、2、2,其他不可约表示例如A、B等不简并。
1,占据规则:
一般要求避免分数占据,例如P是三重简并,因此每个轨道要么占据3个电子要么占据0个电子:
P 6//3
表示α自旋有2个p轨道是满占据的,各占据3个电子,因此总共6个电子,β自旋有一个轨道满占据,因此有3个电子。
如果是Restricted计算,则占据数只能是6的倍数,例如
P 6
2,不符合占据规则的占据造成什么后果?
会导致电子云的对称性低于分子实际对称性。例如F原子,本身是球对称,但是如果总共只有9个电子,则P轨道缺一个电子,例如Pz β为空,则会导致α电子云是球对称,但是β电子云并不是球对称,而是D∞h对称,因此二者叠加到一起也就只是D∞h对称:
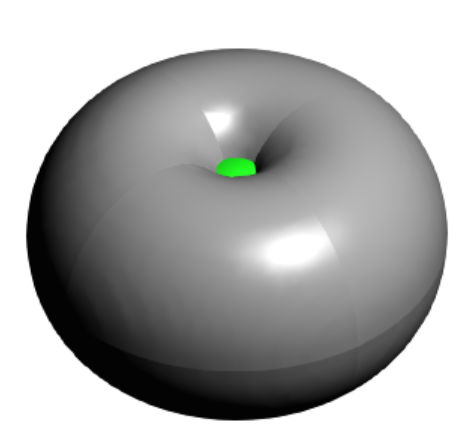
3,如何根据分子的点群与不可约表示,去指定占据
在知道分子点群,但不知道分子的不可约表示时,可以先用ADF做一个单点计算,例如一个三重态的O原子,本来是最高的对称SO3群,但是SO3群只有S、P、D、F等不可约表示简并度分别为1、3、5、7,没有办法指定出一个三重态的整数占据方式来,例如
S 2//2 P 2//0
P只占据2个电子,违背了上面说的占据规则,因此必须降低点群,但是具体降低到哪个点群,就取决于整体的对称性,例如Sr(CO)8,整体是Oh群,因此Sr就适合采用Oh群。这里我们以Oh群为例说明三重态O原子如何占据电子。
首先设置为该点群,进行一个单点计算(对原子设置点群,一般要求将原子设为坐标原点):
 注意这里设置了Core Large,因此冻结了1s电子,1s电子不参与计算,只剩下2s、2p共6个电子。
注意这里设置了Core Large,因此冻结了1s电子,1s电子不参与计算,只剩下2s、2p共6个电子。
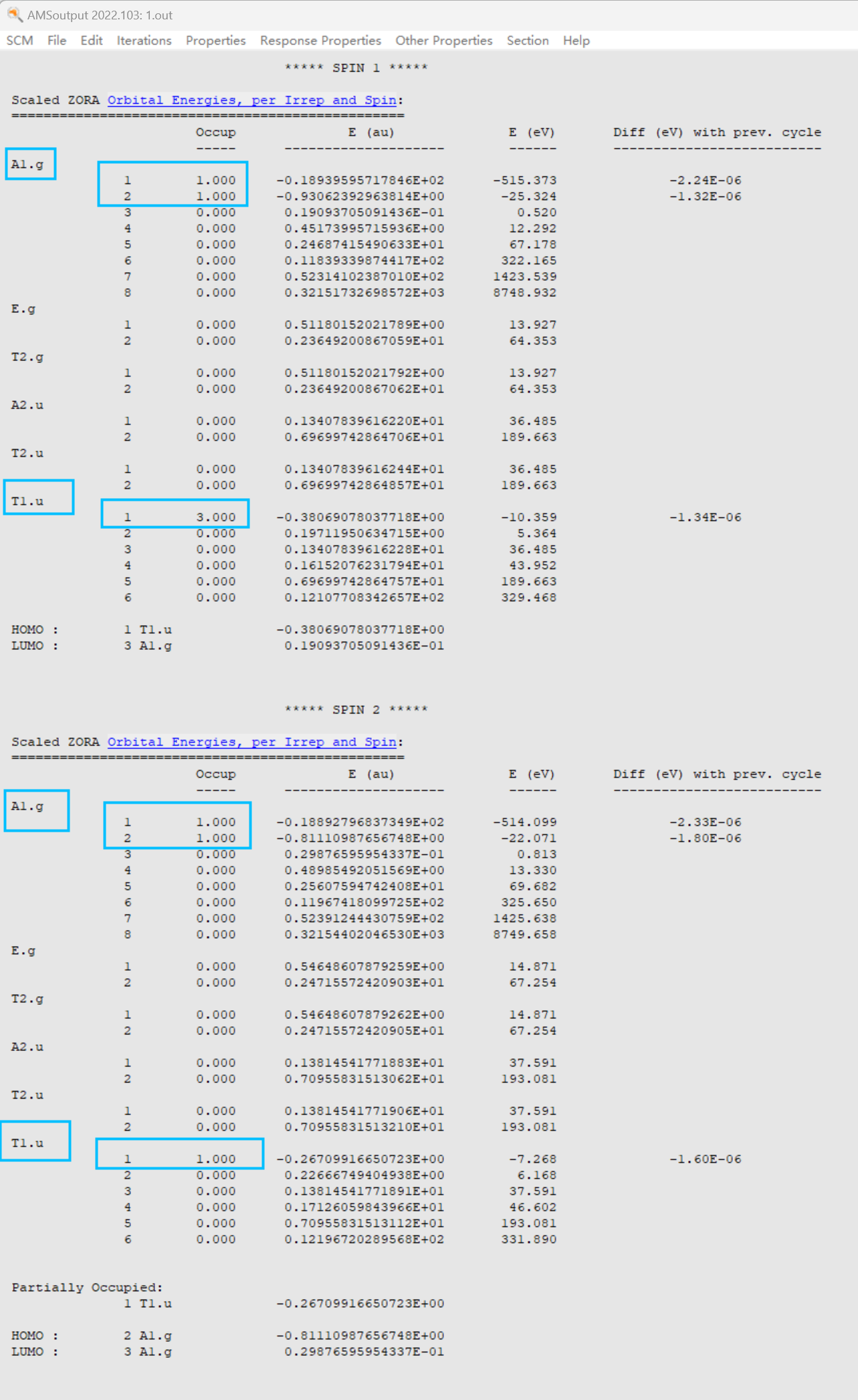
保存并提交作业,计算完毕后,SCM → Output → Properties → Orbital Energies of per Irrep,显示不可约表示有哪些,占据多少电子:
可以看到占据情况为:
A1.g 2//2 T1.u 3//1
前面我们说了T是三重简并,但T1.u的β只有1个电子,显然产生的电子云不符合Oh对称性的,可以调整占据,例如:
A1.g 2//2 A2.u 1//1 E.g 2//0
如此就符合了占据规则(E为二重简并)。在AMSinput中体现为:
但这只是一个道理上的说明,实际上这种占据能量是非常高的,但也从侧面说明三重态O原子不可能以该点群存在。用户可以根据实际情况,尝试其他点群。
常见错误
*.logfile尾部提醒:ERROR DETECTED: Input error: unrecognized entry “a” found in line 10
该体系计算,根本不是C1群,因此根本没有A这个不可约表示,却对A不可约表示指定电子,当然会报错!